- 首页
- 产品
-
信号通路
- 细胞进程相关信号通路(Cellular Processes)
- 细胞的环境信息应答相关信号通路(Environmental Information Processing)
- 人类疾病相关信号通路(Human Diseases)
-
机体系统相关通路研究(Organismal Systems)
- 免疫相关通路(Immune-Related Pathways)
- 造血与凝血相关通路(Hematopoietic & Coagulation-Related Pathways)
- 内分泌与代谢相关通路(Endocrine & Metabolic Pathways)
- 神经相关通路(Neural-Related Pathways)
- 心血管与肌肉相关通路(Cardiovascular & Muscle-Related Pathways)
- 发育与衰老相关通路(Development & Aging-Related Pathways)
- 节律与信号调控相关通路(Rhythm & Signal Regulation Pathways)
- 遗传信息调控相关信号通路(Genetic Information Processing)
- 支持中心
- 联系我们

一、发现溯源与科学定义
纳米抗体(Nanobody, Nb)又称单域抗体(Single-Domain Antibodies, sdAb),其核心功能单位为重链可变区(VHH, variable domain of heavy chain of heavy-chain antibody)。1989 年比利时科学家首次在骆驼科动物血液中发现天然无轻链重链抗体,1993 年 Hamers-Casterman 团队在《自然》杂志明确其特性 —— 重链可变区可脱离恒定区独立存在并维持抗原结合活性,因晶体尺寸仅 2.5nm×4nm、分子量 12-15kDa(约为传统 IgG 抗体的 1/10)而得名 "纳米抗体",且极端环境耐受性更优。
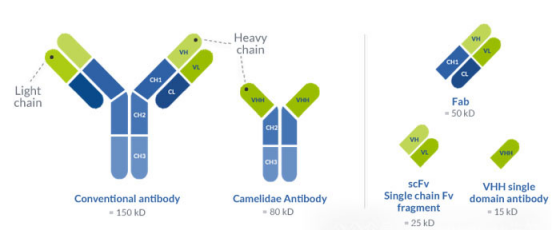
二、核心结构解析与关键特性
(一)独特分子结构
天然缺失轻链,仅由重链可变区(VHH)构成功能核心,其结构具有三大特征:
1 序列特征:含 3 个高变区(CDR1/CDR2/CDR3)与 4 个骨架区(FR1-FR4),FR2 区 4 个脂肪族氨基酸被亲水性残基取代,大幅提升水溶性并避免聚集;
2 结合位点特性:CDR3 区域显著延长(16-18 个氨基酸),可形成凸状、凹槽状或口袋状构象,弥补轻链缺失的结合力损失;
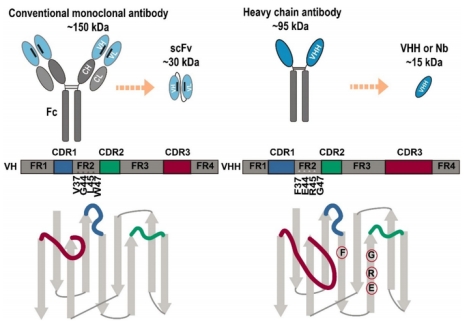
3 稳定性基础:内部存在额外环间二硫键,维系构象稳定并增强抗逆性。
(二)九大核心优势
生物特性 | 具体表现 | 技术价值 |
分子特性 | 分子量 12-15kDa,组织穿透力强,可穿透血脑屏障及肿瘤微环境 | 实现深部病灶靶向,提升药物递送效率 |
免疫安全性 | 与人类 VH 结构同源性达 90%,人源化改造后免疫原性极低 | 降低临床应用免疫排斥风险 |
特异性 | 特异性强,识别蛋白天然构象;CDR3 区长且构象灵活,可识别传统抗体难以结合的隐蔽抗原表位 | 拓展可靶向抗原谱,尤其适用于构象型抗原 |
亲和力 | 解离常数(Kd)可达纳摩至皮摩级,结合特异性与传统抗体相当甚至更优 | 保障诊断与治疗的精准性 |
理化稳定性 | 耐受 pH2-11、85℃高温、蛋白酶及有机溶剂,变性后可重折叠恢复活性 | 支持室温储运,适配口服、雾化等多元给药途径 |
制备便利性 | 可在大肠杆菌、酵母等原核 / 真核系统高效表达,表达量显著高于传统抗体片段 | 降低生产成本,缩短制备周期 |
工程灵活性 | 易于进行人源化改造,可构建双特异性、多价抗体或融合蛋白 | 满足多元化应用需求 |
批次稳定性 | 基因工程重组表达,批次间序列与活性一致性高 | 保障临床应用与工业生产的稳定性 |
筛选效率 | 可通过噬菌体展示文库快速筛选,周期仅数周 | 加速靶点验证与药物研发进程 |
三、主流制备技术与产业化支撑
(一)核心制备流程
目前以噬菌体展示技术为核心,典型流程包括:
抗原免疫:用目标抗原免疫骆驼、大羊驼等宿主,免疫 4-5 次后取血;
文库构建:提取淋巴细胞 RNA,反转录为 cDNA 后扩增 VHH 基因,构建噬菌体展示文库;
筛选纯化:通过多轮淘选获得高亲和力克隆,经原核 / 真核系统表达纯化;
活性验证:采用 ELISA、SPR 等技术验证结合活性与特异性。
(二)产业化技术平台
已建立全人蛋白噬菌体展示纳米抗体文库,形成从 "抗原合成→文库筛选→测序鉴定→重组表达" 的全链条技术体系,目前已完成 200 + 个靶点的纳米抗体开发,可快速获得高品质目标分子。
四、多领域应用场景与最新进展
(一)疾病治疗领域
已上市药物:2018 年全球首个纳米抗体药物 Cablivi(caplacizumab)获批,用于治疗血栓性血小板减少性紫癜;
肿瘤治疗:靶向 EGFR、BCMA 等靶点的纳米抗体 CAR-T 疗法进入临床 Ⅲ 期,部分患者完全缓解期超 15 个月;
神经疾病:2025 年国际团队开发的谷氨酸受体激活型纳米抗体,可通过外周注射改善精神分裂症认知障碍,药效持续超一周;
感染性疾病:抗 SARS-CoV-2 纳米抗体经冻干和气雾化后稳定性良好,已用于鼻腔喷雾剂研发。
(二)诊断检测领域
临床诊断:集成于胶体金试纸、电化学发光平台,用于肿瘤标志物(如 CEA、CA125)、病原体(如新冠病毒、流感病毒)的快速精准检测;
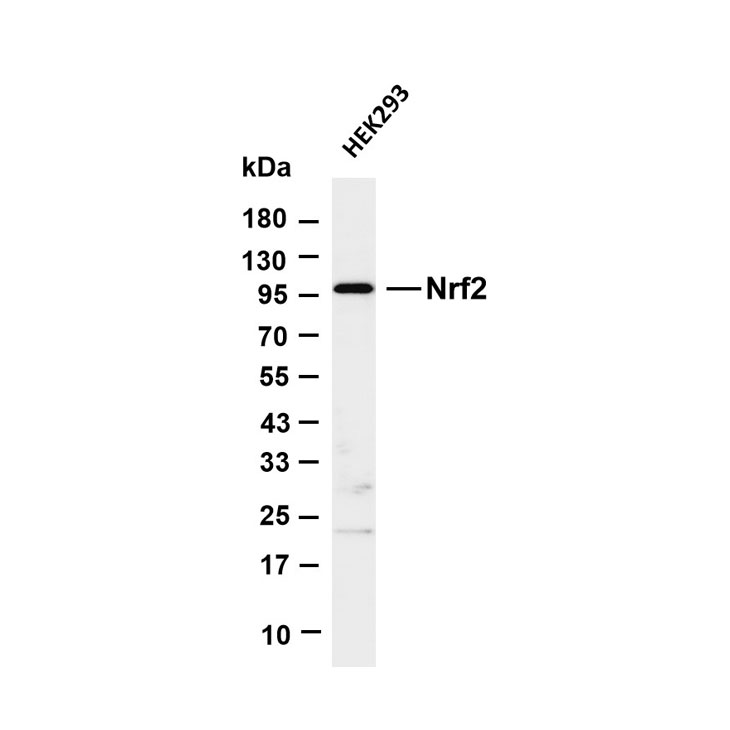
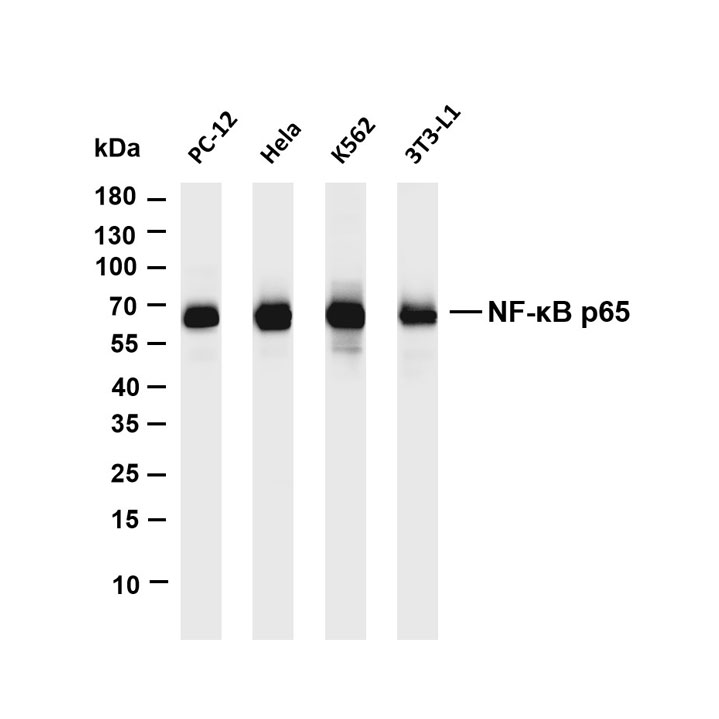
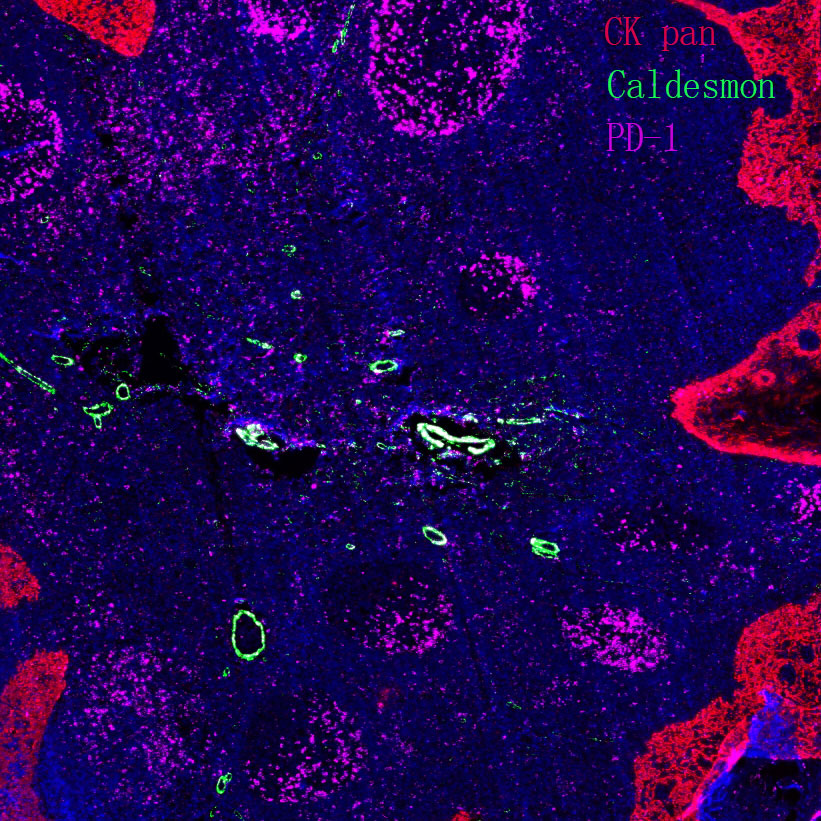
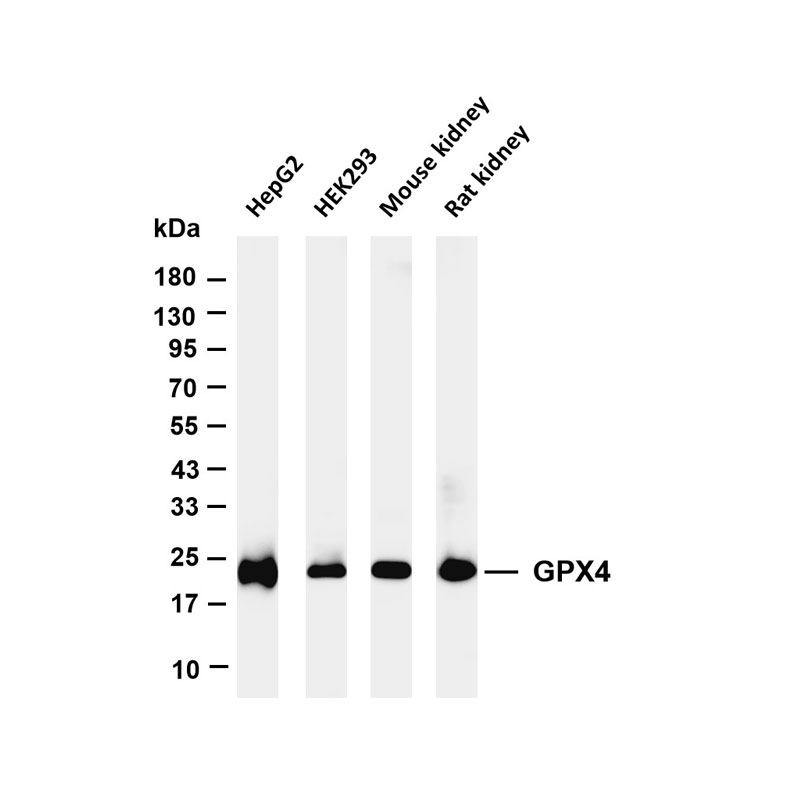
科研工具:适配 FCM、IP、WB、IHC/IF 等技术,实现低丰度蛋白的高灵敏度检测,助力蛋白互作与代谢调控研究。
(三)特色应用方向
活体成像:标记荧光染料或放射性同位素后,实现肿瘤、病原体的多模态成像(光学 / 核磁 / CT),肿瘤 / 背景比显著高于传统抗体;
靶向放疗:作为放射性同位素载体,精准递送至肿瘤细胞,减少正常组织损伤;
药物递送:偶联化疗药物或毒素,实现病变部位精准释放,降低全身毒副作用;
食品安全:开发针对农药残留(杀螟硫磷、腐霉利)、生物毒素的特异性纳米抗体,用于快速检测。
五、发展现状与未来展望
目前全球已有 40 余个纳米抗体候选药物进入研发管线,覆盖癌症、自身免疫病、神经疾病等领域。我国企业在 PD-L1 纳米抗体、CAR-T 疗法等方向进展迅速,部分产品同步开展中美日多中心临床试验。随着千亿级文库构建、高通量筛选技术的突破,以及多特异性纳米抗体、胞内靶向纳米抗体的研发深入,其 "下一代生物技术导弹" 的应用潜力将进一步释放,有望在精准医疗、即时诊断等领域实现颠覆性突破。
Related Resource Links
Related Promotional Journal Downloads