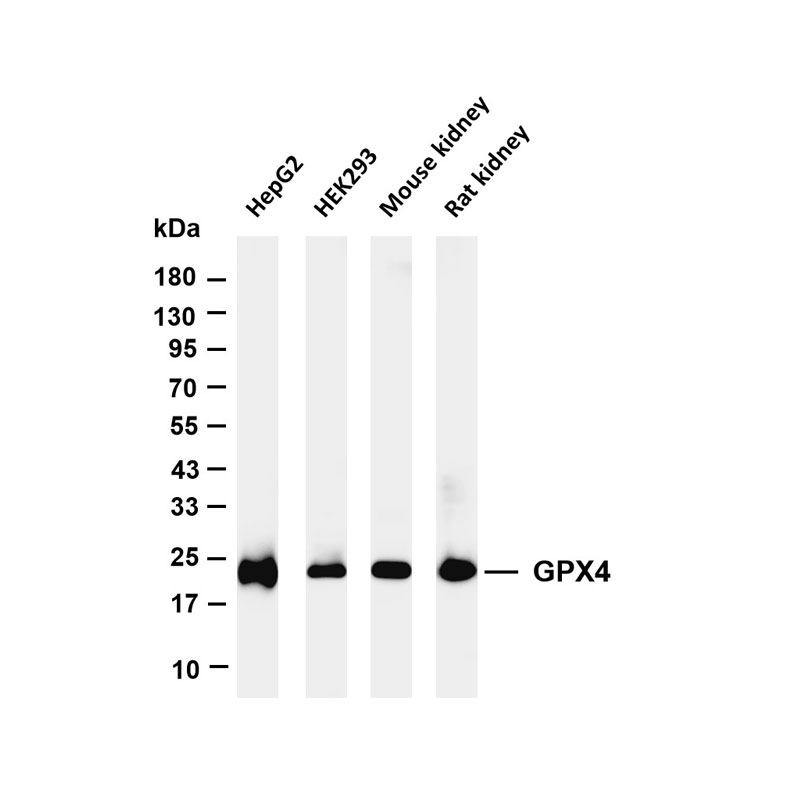
肿瘤作为全球健康重大威胁,涵盖常见高发及难治性癌症类型,其发病机制涉及基因突变、信号通路异常等复杂环节。科研抗体凭借高特异性识别能力,在肿瘤早期筛查、靶向药物研发及免疫逃逸机制解析中发挥关键作用,为肿瘤精准研究与治疗提供核心支撑。
在生命科学多元研究领域,从信号通路调控、细胞器功能解析到免疫机制探索、干细胞应用研究等,抗体均是不可或缺的工具。它支撑 WB、IHC、IF 、CO-IP、ELISA、FCM等核心实验技术,助力科研人员解锁细胞代谢、发育调控、疾病发生等生命奥秘,推动生命科学领域持续突破。未来,随着抗体性能优化与新靶点发现,其将为肿瘤攻克及生命科学进步注入更强动力。
激酶抑制剂(肿瘤靶向治疗的核心利器)
激酶在肿瘤信号通路中扮演关键调控角色,其异常激活会驱动细胞异常增殖、分化及转移。激酶抑制剂通过特异性阻断异常激酶活性,抑制肿瘤细胞生长,是目前肿瘤靶向治疗的重要药物类型,推动了肺癌、乳腺癌等多种癌症的治疗革新。
核心激酶靶标标志物
RTK / 生长因子受体:EGFR、突变型 EGFR、ROS1、ALK、Met、VEGFR、PDGFR。
细胞内激酶:B-Raf、Ras、K-Ras、IRAK、GSK3、c-Jun。
激酶下游信号通路标志物
增殖 / 存活通路:Phospho-Akt、Phospho-p44/42 MAPK(Erk1/2)、Phospho- p38 MAPK、Phospho- MEK1/2。
代谢 / 合成通路:Phospho-p70 S6 Kinase、p70 S6 Kinase。
激酶抑制效果验证标志物
磷酸化激酶:对应靶激酶的磷酸化形式(如 Phospho-EGFR、Phospho-ALK),直接反映激酶活性抑制情况。
下游通路磷酸化蛋白:Phospho-p44/42 MAPK(Thr202/Tyr204)等,间接验证抑制剂对信号传导的阻断效果。
细胞周期的精准调控确保细胞正常分裂,DDR 系统负责修复 DNA 损伤,二者功能异常会导致基因组不稳定,进而诱发肿瘤。
研究该方向可明确肿瘤细胞周期紊乱及 DNA 修复缺陷的机制,为开发靶向细胞周期检查点、DDR 通路的抗癌药物提供理论基础。
细胞周期调控常用标志物
周期检查点分子:CDK4、CDK6、CDK2、Cyclin D1、Cyclin E1、PLK1。
核心调控蛋白:Phospho-Rb(Ser807/811)、Rb。
DNA 损伤应答(DDR)常用标志物
损伤感应与信号传导:ATM、ATR、Phospho-Chk1(Ser345)、Chk1、Phospho-Chk2、Chk2。
修复与凋亡调控:Phospho-p53、p53、MDM2、PARP、Rad51。
衰老相关标志物
周期抑制蛋白:p16 INK4A、p21 Waf1/Cip1。
结构与功能指标:Lamin B1、β- 半乳糖苷酶。
肿瘤细胞为满足快速增殖需求,会发生代谢重编程,表现为糖酵解增强、谷氨酰胺代谢异常等独特代谢表型。
解析肿瘤代谢机制有助于揭示肿瘤细胞的生存策略,为开发针对代谢靶点的抑制剂(如糖酵解抑制剂)及肿瘤营养干预提供新思路。
葡萄糖代谢标志物
转运与分解:Glut1(葡萄糖转运蛋白)、HK2(己糖激酶)、PKM2(丙酮酸激酶)。
信号调控:Phospho-IGF-IR、Phospho- Insulin Receptor β、Phospho-GSK-3β。
脂肪酸与氨基酸代谢标志物
脂肪酸代谢:乙酰 CoA 羧化酶(ACC)、Phospho-ACC(Ser79)、Perilipin-1。
氨基酸代谢:Arginase-1、ASS1、Phospho-BCKDH。
自噬相关标志物
关键分子:LC3B、Phospho-mTOR、Atg13、ULK1、SQSTM1/p62。
该方向聚焦正常细胞向肿瘤细胞转化的分子机制,包括原癌基因激活、抑癌基因失活、肿瘤微环境重塑等关键环节。
明确转化 / 肿瘤发生机制是理解癌症起源的基础,为早期干预肿瘤发生、开发肿瘤预防策略提供核心靶点。
转录因子 / 共激活剂标志物
关键分子:Phospho-STAT3、c-Myc、GLI、p65、PAX5。
信号转导通路标志物
关键通路分子:Phospho-SMAD2/3、TGF-β、β-Catenin、YAP/TAZ、LATS1、DLL3、Notch1/2/3。
EMT 核心生物标志物
上皮 / 间质表型分子:E-Cadherin(上皮)、Vimentin、α-Smooth Muscle Actin、Fibronectin(间质)、Vinculin。
凋亡机制紊乱是肿瘤细胞存活的重要原因,肿瘤细胞常通过逃逸凋亡实现无限增殖。
靶向凋亡研究旨在开发药物激活肿瘤细胞凋亡通路,或抑制其抗凋亡机制,是癌症治疗的重要方向,如 Bcl-2 家族抑制剂已在血液系统肿瘤治疗中取得显著成效。
Intrinsic Apoptosis Pathway Biomarkers
Anti-Apoptotic Proteins: Bcl-2, Bcl-xL, Mcl-1
Pro-Apoptotic Proteins: Bax, Bim, Bad, Puma, Noxa
内在凋亡通路标志物
抗凋亡蛋白:Bcl-2、Bcl-xL、Mcl-1
促凋亡蛋白:Bax、Bim、Bad、Puma、Noxa
外在凋亡通路标志物
死亡受体及配体:TRAIL、DR4、DR5、TNF、TNF-R1、TNF-R2、FasL、Fas
Caspase 激活剂及凋亡执行标志物
激活剂:Smac/Diablo、XIAP、c-IAP1、c-IAP2、Survivin、Livin
执行分子:Cleaved Caspase-3、Cleaved Caspase-9、Cleaved PARP
表观遗传修饰(DNA 甲基化、组蛋白修饰等)通过调控基因表达参与肿瘤发生,其异常会导致原癌基因激活或抑癌基因沉默。
研究表观遗传调节机制可揭示肿瘤发生的表观遗传特征,为开发表观遗传靶向药物(如 DNA 甲基转移酶抑制剂)提供理论支撑。
甲基化与去甲基化调控标志物
组蛋白调节:Ezh2、LSD1、H3K27me3
DNA 调节:DNMT、TET、5 - 甲基胞嘧啶(5-mC)、5 - 羟甲基胞嘧啶(5-hmC)、N6 - 甲基腺苷(m6A)、METTL3、FTO
乙酰化与脱乙酰化调控标志物
组蛋白调节:CBP、p300、H3K27ac、HDAC
组蛋白突变标志物
突变型组蛋白:H3K27M、H3K36M、H3K9M
修饰相关:H3K27me3、H3K36me3、H3K9me3
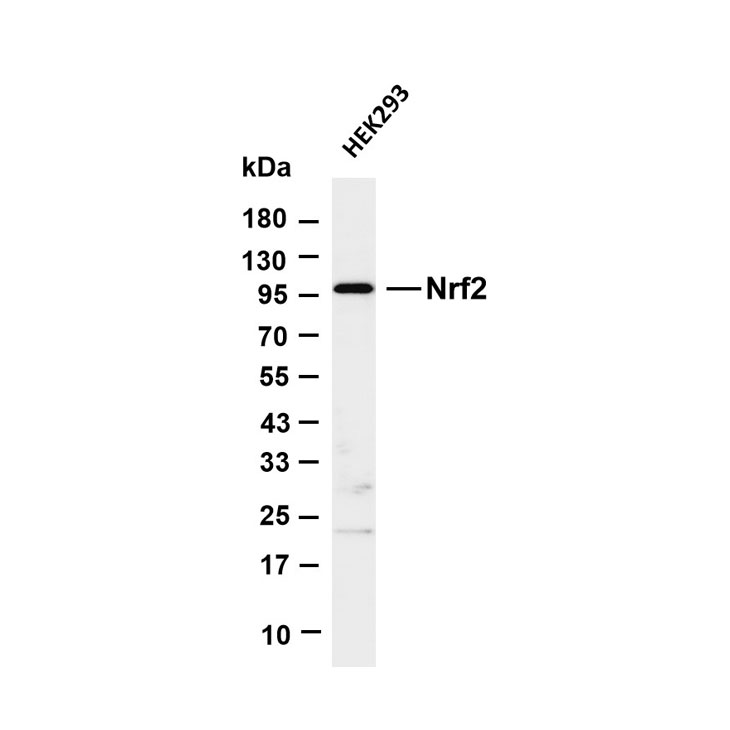
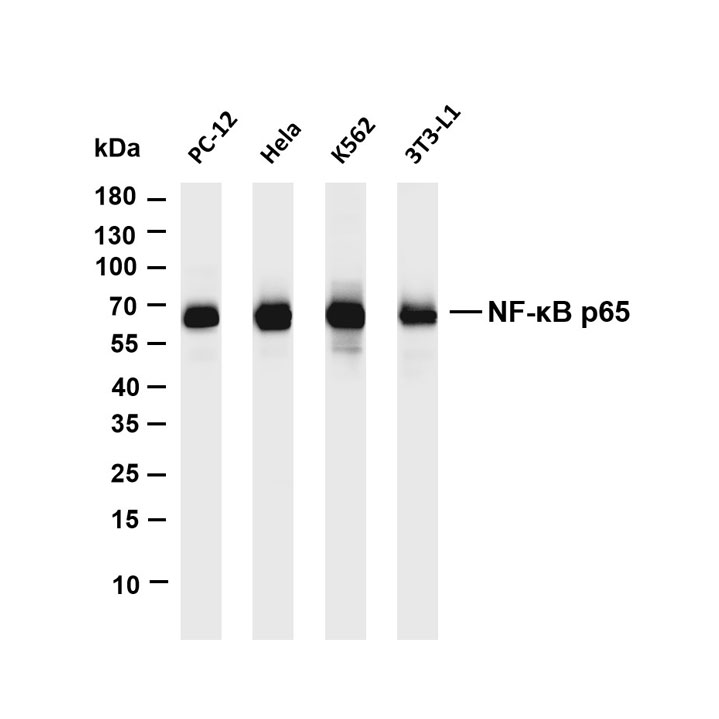
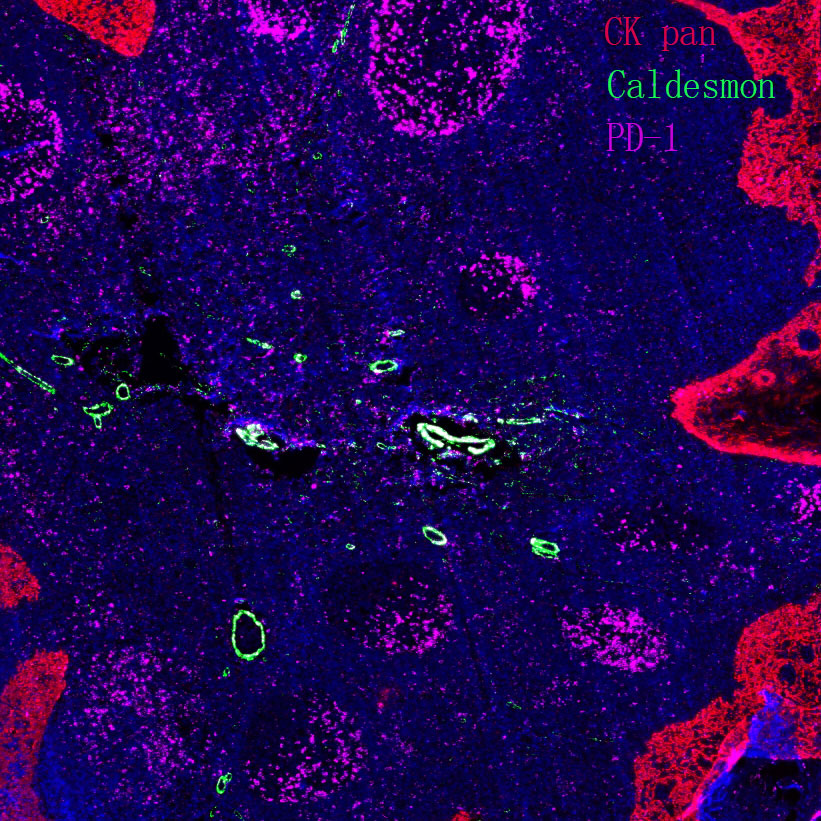
常用肿瘤生物标志物
修饰抗体具有终极表位特异性、高灵敏度、多维严格验证系统和准确捕捉蛋白质功能动态变化的特点。